Indhold
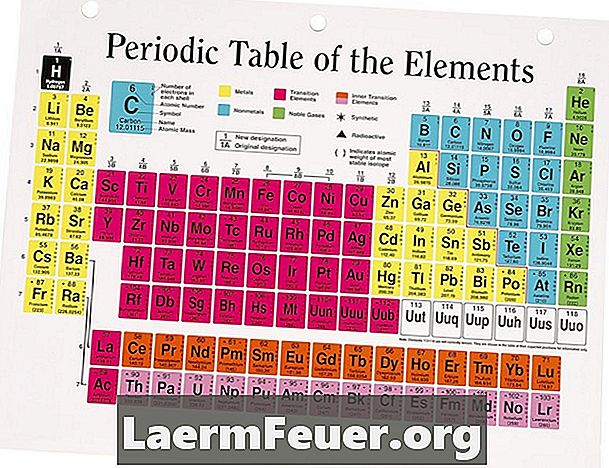
Valenselektroner er elektronerne i det yderste lag, som et atom kan fylde. De er betydelige, da de normalt er involveret i kemiske reaktioner. Den periodiske tabel med elementer er en praktisk reference til hurtigt at bestemme antallet af valenselektroner i et atom. Det skal imidlertid bemærkes, at mange elementer, som mest er overgangsmetaller og endda nogle nonmetals, kan have flere valence tilstande afhængigt af den specifikke forbindelse.
retninger
-
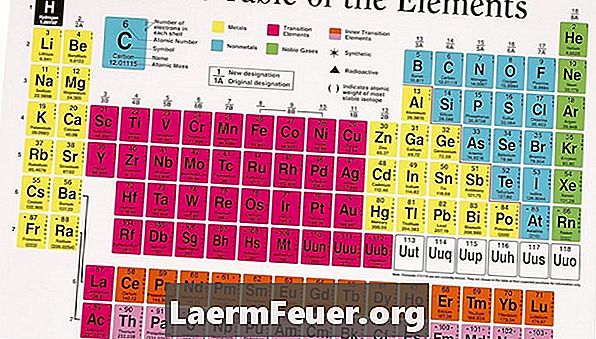
Find elementet i det periodiske bord. De er placeret i bordet med atomnummer fra venstre til højre, top til bund. Arrangementet af elementerne i linjer svarer til egenskaberne, der er delt mellem dem i en given kolonne, der er væsentligt reguleret af ligheder i arrangementet af disse elektroner.
-
Identificer den kolonne, hvor elementet er placeret. Hver kolonne er navngivet med et nummer nær dets top. Nummereringssystemet, der i øjeblikket accepteres af IUPAC, er sekventielt nummereret fra 1 til 8. Tidligere navngav IUPAC kolonne 1A, 2A, 3A osv. Mens de nye periodiske tabeller skal eftermonteres til det nye system, kan de gamle bruge den tidligere nomenklatur.
-
Tæl antallet af kolonner fra venstre mod højre, ignorer overgangsmetallerne og den sidste kolonne til højre. Skriv det som antallet af valenselektroner. For eksempel, ved at bruge det foregående nummereringssystem, skriv simpelthen det romerske tal i kolonnen betegnet som valenselektronumre, for elementer i gruppe IA, IIA, IIIA, IVA, VA, VIA og VIIA.
-
Skriv nul for antallet af valenselektroner for elementerne i gruppe 18 (tidligere kaldet gruppe VIIIA). Disse elementer præsenterer det yderste elektronlag fyldt og er generelt ikke involveret i kemiske reaktioner.
-
Skriv ordet "varierer" for de elementer, der er placeret i overgangsmetalblokken i det periodiske bord, da arrangementet af elektroner i disse elementer tillader dem i et inderste lag at deltage i kemiske reaktioner. Dette får dem til at synes at have en valens, der ændrer sig i de forskellige reaktioner. Jern, for eksempel reagerer undertiden ved hjælp af to elektroner, og en anden tre, hvilket giver det en tilsyneladende valens på to eller tre.
Hvad du har brug for
- Periodiske tabel over elementer