Indhold
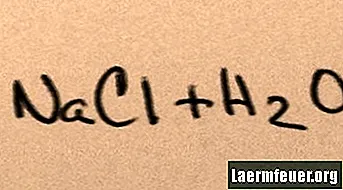
Når salt tilsættes vand, opløses det i dets komponentmolekyler, indtil de maksimale saltioner, som vandet kan understøtte, flyder omkring hydrogen- og iltmolekylerne. Når dette sker, kaldes løsningen "mættet". Når mere salt opløses, kolliderer natrium- og chloridioner med hinanden og rekombineres i saltkrystaller. Dette fænomen er kendt som "udfældning", fordi det dannede faste stof falder til bunden af vandet. Salte er "hydrofile", dvs. de tiltrækkes af vand. Denne attraktion letter en velkendt form for nedbør: regndråber dannes omkring små krystaller af salt i skyerne, hvilket gør det smag lidt salt.
Det basale

Elektrolytter

Salt leder ikke elektricitet i fast tilstand, men i flydende (flydende) tilstand danner den en løsning, der kan lede elektricitet meget godt. Ledningsevne afhænger af den anvendte salttype, men disse væsker, kaldet elektrolytopløsninger, er fremragende bærere af forbindelser, som den menneskelige krop har brug for. De elektriske impulser, der genereres af hjernen, producerer frit ilt, som bruges af blodet. Saltmolekylerne klassificeres i elektrolytter (natrium, kalium eller calcium) og klorider i opløsning: kloridet pumpes af blodet og nyrerne i urinen, og elektrolytterne fordeles gennem det neuromuskulære system i en proces, som atleter kalder rehydrering.
Colligative egenskaber

Enhver opløsning adskiller sig fra den oprindelige sammensætning, fordi tilsætningen af molekyler, selv når de ikke danner nye forbindelser, ændrer væskens molekylvægt og påvirker dens egenskaber. Saltvand er tættere end rent vand og fryser også langsommere. Når det fryser, migrerer saltet imidlertid til væskens grænser, hvilket gør det tungere og mere mættet og sænker derefter dets frysepunkt. I den anden ende af tilstanden af stof, jo tættere saltvandet er, desto mere varme kræver det at fordampe, indtil vandet løber tør og efterlader et saltlag. Kokke venter på, at vandet i gryden koger for at tilsætte salt for ikke at forsinke opvarmningen. Disse kvaliteter, kendt som "kolligative egenskaber", hjælper forskere med at bestemme molekylvægten af saltvand. Hvis væskens masse, atmosfæriske tryk og kogepunkt kan måles, kan forskere trække vandets molekylvægt for at finde ud af, hvilke salte der er til stede.