
Indhold
Natriumacetat-trihydrat er en almindelig og billig forbindelse, der anvendes til forskellige anvendelser i fødevarer, industrier og laboratorier. Den anvendes til betning, garvning, som buffer og som hovedkomponent i elektriske kompresser. Natriumacetat studeres til brug ved denitrificering af spildevand som en bestanddel af nematicider.
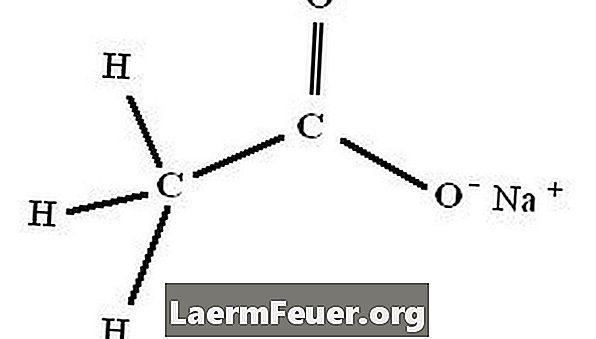
forberedelse
Natriumacetat-trihydrat, kemisk formel NaC2H3O2.3H20, dannes øjeblikkeligt ved reaktionen mellem eddikesyre (eddike) og natriumhydroxid, natriumcarbonat eller natriumbicarbonat.
Navn og formel
Det videnskabelige navn for eddikesyre er ethanoalkohol. Af denne grund kaldes natriumacetat undertiden natriumethanoat.
Organiske kemikalier skriver strukturen af natriumacetat som NaCl2H3O2.3H2O. I nogle situationer bruger de dog den forkortede notation "NaAc".
Fødevarebrug
I et et til et forhold kan natriumacetat og eddikesyre krystalliseres i et produkt kaldet natriumdiacetat. Dette produkt er meget nyttigt i fødevareindustrien, fordi det er et fast stof med næsten ingen lugt, men "in situ" nedbryder den til dets komponenter. Både natriumacetat og diacetat var GRAS ("generelt anerkendt som sikker") af Food and Drug Administration.
Natriumacetat anvendes i kød- og fjerkræindustrien for at forbedre smagen. Diacetat anvendes til et lignende formål og som en væksthæmmer af patogener.
Medicinsk brug
Natriumacetat i medicin bruges til at genvinde elektrolytter. Det tjener også som et diuretikum.
Den mest interessante anvendelse af det er i elektriske kompresser. Natriumacetat-trihydrat indeholder tre vandmolekyler af krystallisation. Varm det til 58 grader Fahrenheit, og disse farvande vil blive frigivet fra krystal. De opløser det dehydrerede natriumacetat, idet det faste stof udskiftes med en opløsning. Denne opløsning kan afkøles uden omkrystallisation til stuetemperatur. Når det ønskes, med tilstrækkelig stimulering, kan denne væske blive tvunget til at krystallisere igen. Krystallisationen frigiver varme ved opvarmning af den ønskede kropsdel.
Industriel anvendelse
Natriumacetat er et alkalisk salt, produktet af reaktionen af en stærk base med en svag syre. Derfor gør dens basicitet, såvel som dens lave omkostninger, det attraktivt i neutraliseringen af industrielle mineralsyrer af udledning.
I skadedyrsbekæmpelse er natriumacetat under undersøgelse til brug som en bestanddel af nematicider. Nematoider kan tiltrækkes af natriumacetat som om det var en agn, ligesom insekter kan tiltrækkes af feromoner.